PRODUCTOS
LA MEJOR CALIDAD Y GRAN VARIEDAD.
Lo que Orthograft Ofrece
PRODUCTOS POR FAMILIA
En esta sección encontrarás nuestros productos catalogados por familia o clase de producto.
- BioSponge - BioSponge
- BioDBM - Matriz Ósea Desmineralizada
- Diáfisis y Hemidiáfisis - Diáfisis Femoral
- - Hemidiáfisis Femoral
- - Diáfisis Tibial
- - Diáfisis Humeral
- - Diáfisis de Peroné
- - Diáfisis Radial
- - Diáfisis de Cúbito
- Hueso Esponjoso - Chip Granulado Esponjoso
- - Chips Cubos de Esponjosa
- - Chips Granulado Corticoesponjoso
- - Polvo de Hueso
- - Bloque Esponjoso
- Cuña Ósea - Cuñas Óseas
- Cabeza Femoral - Cabeza Femoral Sin Cartílago
- Bloques y Tiras - Bloque de Iliaco Tricortical
- - Tira de Iliaco Tricortical
- - Tira de Iliaco Bicortical
- - Tira Barra Cortical
- Tendones - Tendón Procesado Biograft
- - Tendón de Aquiles
- - Tendón Hueso HTH
- - Fascia Lata
- BioXiliumQ - Matriz dérmica acelular
- BioXiliumH - Matriz dérmica acelular
- BioBrick - Cartílago Procesado
BioSponge
Registro Sanitario: 0956C2013SSA
Descripción
- BioSponge® es un implante innovador que se comprime como una esponja hasta en 1/3 de su tamaño.
- BioSponge® gracias a su capacidad de memoria plástica regresa a su forma original sin comprometer su estructura; no se rasga, no se rompe.
- BioSponge® tiene potencial osteoinductor; se procesa utilizando métodos que permiten la preservación de las proteínas óseas morfogenéticas; encargadas de inducir a las células mesenquimales a diferenciarse en células óseas.
- BioSponge® tiene capacidad osteoconductora; su estructura trabecular le permite actuar como un andamiaje o como una estructura que cuenta con una porosidad interconectada capaz de apoyar a la neovascularización, la formación de la unidad osteoide y el desarrollo de nuevo hueso.
- BioSponge® es un implante derivado de tejido óseo humano, es estéril y está libre de pirógenos. Se obtiene a partir del procesamiento de tejido óseo cadavérico que ha sido tratado con una sustancia ácida desmineralizante que genera un material compresible.
- BioSponge® es un producto liofilizado que puede almacenarse a temperatura ambiente por un periodo prolongado aguardando su requerimiento quirúrgico.
Aplicaciones
El BioSponge® está indicado como una ayuda en procedimientos quirúrgicos del área dental, ortopedia, traumatología, neurología, maxilofacial, dental, como en los siguientes procedimientos:
- En la reconstrucción de defectos mandibulares o perdidas de tejido óseo en mandíbula o maxilar.
- Relleno de cavidades producidas por osteomielitis, tumores.
- En defectos de tibia, fémur y cadera en prótesis de revisión.
- Relleno en defectos de prótesis primarias.
- Artrodesis de columna cervical, lumbar, torácica.
- Relleno de cajas cervicales.
- Relleno de cajas lumbares.
- Seudoartrosis de cualquier hueso.
- Consolidación viciosa y osteotomías correctivas.
- Artrodesis de muñeca, de hombro, de codo, cadera, rodilla, tobillo, metatarsianos, metacarpianos, falanges de los dedos de la mano y pies. Relleno de defectos de fracturas.
- Relleno de fracturas de los cuerpos vertebrales cervicales, torácicas y lumbares.
Código de Producto
- 16100510 Bloque de hueso desmineralizado > 10 x > 10 mm
- 16100515 Bloque de hueso desmineralizado > 15 x > 15 mm
- 16100501 Bloque de hueso desmineralizado > 10 x > 25 mm
Matriz Ósea Desmineralizada
Registro Sanitario: 1607C2011 SSA
Descripción
- BioDBM® es una matriz ósea desmineralizada obtenida de hueso cortical humano con potencial osteoinductivo.
- BioDBM® es un producto seguro, preparado mediante un proceso aséptico con esterilización terminal y es presentado como polvo liofilizado en un contenedor para su fácil preparación. Esta presentación permite que pueda ser preparado en gel o masilla (putty) de acuerdo a las necesidades del cirujano, inclusive en el mismo evento quirúrgico.
- BioDBM® tiene una caducidad de 36 meses y se conserva a temperatura ambiente (16 a 37°C).
Aplicaciones
El BioDBM® está indicado como una ayuda en procedimientos quirúrgicos del área dental, ortopedia, traumatología, neurología, maxilofacial, dental, como en los siguientes procedimientos:
- En tratamiento de tumores óseos que provocan defectos en los huesos o cavidades que requieran su relleno
- En tratamientos de fracturas que provocan perdida de tejido óseo debido al traumatismo que la provocó
- En la reconstrucción de defectos mandibulares o perdidas de tejido óseo en mandíbula o maxilar
- En los defectos alveolares en maxilares o mandíbula que requiera un apoyo mayor de tejido óseo
- En el tratamiento de defectos de cráneo posterior a traumatismo y perdida de tejido óseo
- Como complemento a las cirugías de columna en las instrumentaciones posteriores o anteriores y que se busca artrodesar esos segmentos
Código de Producto
- 16100650- Matriz ósea desmineralizada 0.5cc
- 16100601- Matriz ósea desmineralizada 1cc
- 16100602- Matriz ósea desmineralizada 2cc
- 16100600- Matriz ósea desmineralizada 2.5cc
- 16100603- Matriz ósea desmineralizada 3cc
- 16100605- Matriz ósea desmineralizada 5cc
- 16100610- Matriz ósea desmineralizada 10cc
Diáfisis Femoral
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso femoral.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 113 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 113 milímetros, producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Tumores: Perdida masiva de tejido
- Clavo centromedular
Código de Producto
- 16631040- Diáfisis femoral 38-42 mm
- 16631050- Diáfisis femoral 48-52 mm
- 16631060- Diáfisis femoral 58-62 mm
- 16631070- Diáfisis femoral 68-77 mm
- 16631080- Diáfisis femoral 78-87 mm
- 16631090- Diáfisis femoral 88-97 mm
- 16632010- Diáfisis femoral 98-102 mm
- 16632012- Diáfisis femoral 103-113 mm
- 16632014- Diáfisis femoral 114-147 mm
- 16632015- Diáfisis femoral 148-152 mm
- 16632016- Diáfisis femoral 153-197 mm
- 16632020- Diáfisis femoral 198-202 mm
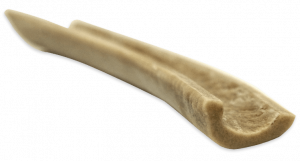
Hemidiáfisis Femoral
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso femoral.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 120 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 120 milímetros: producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Cirugía de revisión
Código de Producto
- 16632110- Hemidiáfisis med/lat 98-102 mm
- 16632113- Hemidiáfisis med/lat 103-147 mm
- 16632115- Hemidiáfisis med/lat 148-152 mm
- 16632118- Hemidiáfisis med/lat 153-197 mm
- 16632120- Hemidiáfisis med/lat 198-202 mm
Diáfisis Tibial
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso de la tibia.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 113 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 113 milímetros, producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Tumores: perdida masiva de tejido
- Clavo centromedular
Código de Producto
- 16781040- Diáfisis tibial 38-42 mm
- 16781050- Diáfisis tibial 48-52 mm
- 16781060- Diáfisis tibial 58-62 mm
- 16781070- Diáfisis tibial 68-77 mm
- 16781080- Diáfisis tibial 78-87 mm
- 16781090- Diáfisis tibial 88-97 mm
- 16782010- Diáfisis tibial 98-102 mm
- 16782012- Diáfisis tibial 103-113 mm
- 16782015- Diáfisis tibial 148-152 mm
- 16782017- Diáfisis tibial 153-197 mm
Diáfisis Humeral
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso humeral.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 120 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 120 milímetros, producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Tumores: perdida masiva de tejido
- Cirugía de revisión
- Clavo centromedular
Código de Producto
- 16691060- Diáfisis humeral 58-62 mm
- 16691070- Diáfisis humeral 68-77 mm
- 16691080- Diáfisis humeral 78-87 mm
- 16691090- Diáfisis humeral 88-97 mm
- 16692010- Diáfisis humeral 98-147 mm
- 16692015- Diáfisis humeral >148 mm
Diáfisis de Peroné
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso peroné.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 120 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 120 milímetros, producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Cirugía columna: corperectomía
- Tumores: perdida masiva de tejido
Código de Producto
- 16661030- Diáfisis peroné 28-32 mm
- 16661040- Diáfisis peroné 38-42 mm
- 16661045- Diáfisis peroné 43-47 mm
- 16661050- Diáfisis peroné 48-52 mm
- 16661060- Diáfisis peroné 58-62 mm
- 16661070- Diáfisis peroné 63-77 mm
- 16661080- Diáfisis peroné 78-82 mm
- 16661090- Diáfisis peroné 83-97 mm
- 16662010- Diáfisis peroné 98-105 mm
- 16662012- Diáfisis peroné 106-120 mm
- 16662014- Diáfisis peroné 121-147 mm
- 16662015- Diáfisis peroné 148-155 mm
Diáfisis Radial
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso del radio.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 120 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 120 milímetros, producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Cirugía columna: corperectomía
- Tumores: perdida masiva de tejido
Código de Producto
- 16751060- Diáfisis radial 58-62 mm
- 16751070- Diáfisis radial 68-77 mm
- 16751080- Diáfisis radial 78-87 mm
- 16751090- Diáfisis radial 88-97 mm
- 16752010- Diáfisis radial 98-147 mm
Diáfisis de Cúbito
Registro Sanitario: 0888C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido de la zona diafisaria del hueso del cúbito.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto con una longitud hasta 120 milímetros, producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
- Producto con una longitud superior a 120 milímetros, producto congelado con una caducidad de 48 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de fracturas por perdida de sustancia ósea
- Cirugía columna: corperectomía
- Tumores: perdida masiva de tejido
Código de Producto
- 16791060- Diáfisis de cúbito 58-62 mm
- 16791070- Diáfisis de cúbito 68-77 mm
- 16791080- Diáfisis de cúbito 78-87 mm
- 16791090- Diáfisis de cúbito 88-97 mm
- 16792010- Diáfisis de cúbito 98-147 mm
- 16792015- Diáfisis de cúbito >147 mm
Chip Granulado Esponjoso
Registro Sanitario: 1374C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en un 70% de sales inorgánicas y en un 30% de matriz orgánica. La parte orgánica está conformada en más de 90% por fibras de colágeno, que se agrupan en forma especializada para originar la matriz ósea. La parte inorgánica está formada por cristales de calcio y fósforo conocidos como Hidroxiapatita (HTA).
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Hueso esponjoso con un tamaño de partícula de 1 a 4 milímetros.
- Producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos óseos y cavidades óseas en procedimientos quirúrgicos en el área de traumatología y ortopedia.
- Tumores
- Quistes
- Cirugía de Columna
- Retardo de Consolidación
- Pseudoartrosis
Código de Producto
- 16100010- Granulado de esponjoso ( <4 mm) 10
- 16100015- Granulado de esponjoso ( <4 mm) 15cc
- 16100030- Granulado de esponjoso ( <4 mm) 30cc
- 16100060- Granulado de esponjoso ( <4 mm) 60cc
- 16100090- Granulado de esponjoso ( <4 mm) 90cc
Chips Cubos de Esponjosa
Registro Sanitario: 1374C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en un 70% de sales inorgánicas y en un 30% de matriz orgánica. La parte orgánica está conformada en más de 90% por fibras de colágeno, que se agrupan en forma especializada para originar la matriz ósea. La parte inorgánica está formada por cristales de calcio y fósforo conocidos como Hidroxiapatita (HTA).
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Hueso esponjoso con un tamaño de partícula de 4 a 6 milímetros.
- Producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos óseos y cavidades óseas en procedimientos quirúrgicos en el área de Traumatología y Ortopedia.
- Tumores
- Quistes
- Cirugía de Columna
- Retardo de Consolidación
- Pseudoartrosis
Código de Producto
- 16100205- Chips cubos de esponjoso (4-6 mm) 5cc
- 16100210- Chips cubos de esponjoso (4-6 mm) 10cc
- 16100215- Chips cubos de esponjoso (4-6 mm) 15cc
- 16100230- Chips cubos de esponjoso (4-6 mm) 30cc
- 16100260- Chips cubos de esponjoso (4-6 mm) 60cc
- 16100290- Chips cubos de esponjoso (4-6 mm) 90cc
Chips granulado corticoesponjoso

Registro Sanitario: 1374C2005 SSA
Código de Producto
- 16110001- Chips granulado corticoesponjoso 1cc
- 16110005- Chips granulado corticoesponjoso 5cc
- 16110010- Chips granulado corticoesponjoso 10cc
- 16110115- Chips granulado corticoesponjoso 15cc
- 16110130- Chips granulado corticoesponjoso 30cc
- 16110160- Chips granulado corticoesponjoso 60cc
Polvo de Hueso
Registro Sanitario: 1374C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en un 70% de sales inorgánicas y en un 30% de matriz orgánica. La parte orgánica está conformada en más de 90% por fibras de colágeno, que se agrupan en forma especializada para originar la matriz ósea. La parte inorgánica está formada por cristales de calcio y fósforo conocidos como Hidroxiapatita (HTA).
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Hueso en polvo con un tamaño de partícula de 500 a 800 uM.
- Producto liofilizado con una caducidad de 24 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos óseos y cavidades óseas en procedimientos quirúrgicos del área dental y maxilofacial.
Código de Producto
- 16140300- Hueso en polvo cortical 1cc (0.5/0.5)
Bloque Esponjoso
Registro Sanitario: 1374C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en un 70% de sales inorgánicas y en un 30% de matriz orgánica. La parte orgánica está conformada en más de 90% por fibras de colágeno, que se agrupan en forma especializada para originar la matriz ósea. La parte inorgánica está formada por cristales de calcio y fósforo conocidos como Hidroxiapatita (HTA).
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Bloque óseo conformado por hueso trabecular obtenido generalmente de las epífisis de huesos largos: fémur, húmero, tibia.
- Producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos óseos y cavidades óseas en procedimientos quirúrgicos en el área de Traumatología y Ortopedia.
- Tumores
- Quistes
- Cirugía de Columna
- Retardo de Consolidación
- Pseudoartrosis
Código de Producto
- 16260130- Bloque de esponjoso 13-17 mm x 13-17 mm
- 16260230- Bloque de esponjoso >18-22 mm x >18-22 mm
- 16260330- Bloque de esponjoso >23-27 mm x >23-27 mm
- 16260399- Bloque de esponjoso > 24 mm
Cuñas Óseas
Registro Sanitario: 1297C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, clase III, producto estéril, libre de pirógenos.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Hueso cortical obtenido a partir de la diáfisis de hueso de femur, peroné, radio y cúbito.
- Producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Cirugía de columna.
- Elongaciones.
Código de Producto
- 16631012 Cuña femoral 12 mm
- 16631014 Cuña femoral 14 mm
- 16631015 Cuña femoral 15 mm
- 16631016 Cuña femoral 16 mm
- 16661106 Cuña peroné 5.5 – 6.4 mm
- 16661107 Cuña peroné 6.5 – 7.4 mm
- 16661108 Cuña peroné 7.5 – 8.4 mm
- 16661109 Cuña peroné 8.5 – 9.4 mm
- 16661110 Cuña peroné 9.5 – 10.4 mm
- 16661111 Cuña peroné 10.5-12.0 mm
- 16751006 Cuña radial 6 mm
- 16751008 Cuña radial 8 mm
- 16751010 Cuña radial 10 mm
- 16751012 Cuña radial 12 mm
- 16791006 Cuña de cúbito 6 mm
- 16791008 Cuña de cúbito 8 mm
- 16791010 Cuña de cúbito 10 mm
- 16791012 Cuña de cúbito 12 mm
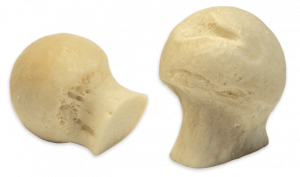
Cabeza Femoral Sin Cartílago

Registro Sanitario: 0067C2006 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Constituido en su mayor parte por sustancia ósea, con matriz de hueso esponjoso y superficie de hueso cortical proveniente de la cabeza femoral.
- Producto congelado con una caducidad de 36 meses.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Revisión de cadera
Código de Producto
- 16620100- Cabeza femoral sin cartílago
Bloque de Iliaco Tricortical
Registro Sanitario: 1359C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en su mayor parte por sustancia ósea, con matriz de hueso esponjoso y superficie de hueso cortical proveniente de la cresta iliaca.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos y cavidades óseas en procedimientos quirúrgicos, en traumatología, ortopedia y cirugía maxilofacial.
- Espaciador para cuerpo vertebral
- Adelantamiento patelar
- Reconstrucción de meseta tibial
- Fracturas por colapso
- Osteotomía pélvica
Código de Producto
- 16310101- Bloque iliaco tricortical 7-10 x >15 x ≥8mm
- 16310102- Bloque iliaco tricortical > 11-16 x >15x ≥8mm
- 16310103- Bloque iliaco tricortical > 17-20 x >15x ≥8mm
Tira de Iliaco Tricortical
Registro Sanitario: 1359C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en su mayor parte por sustancia ósea, con matriz de hueso esponjoso y superficie de hueso cortical proveniente de la cresta iliaca.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto liofilizado con una caducidad de 36 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos y cavidades óseas en procedimientos quirúrgicos, en traumatología y ortopedia.
- Espaciador para cuerpo vertebral
- Adelantamiento patelar
- Reconstrucción de meseta tibial
- Fracturas por colapso
- Osteotomía pélvica
Código de Producto
- 16330030- Tira iliaco tricortical 28 – 45 x ≥24 x >8mm
Tira de Iliaco Bicortical
Registro Sanitario: 1359C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Constituido en su mayor parte por sustancia ósea, con matriz de hueso esponjoso y superficie de hueso cortical proveniente de la cresta iliaca.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto liofilizado con una caducidad de 36 meses y que puede ser almacenado a temperatura ambient.
Aplicaciones
- Indicado para relleno de defectos y cavidades óseas en procedimientos quirúrgicos, en traumatología y ortopedia.
- Espaciador para cuerpo vertebral
- Adelantamiento patelar
- Reconstrucción de meseta tibial
- Fracturas por colapso
- Osteotomía pélvica
Código de Producto
- 16320101- Tira Iliaco bicortical 8 – 15 x ≥15 x ≥ 10mm
- 16320102- Tira Iliaco bicortical ≥16 – 25 x ≥ 15 x ≥ 10mm
- 16320103- Tira Iliaco bicortical ≥ 25 x ≥15 x ≥ 10mm
Tira Barra Cortical
Registro Sanitario: 1359C2005 SSA
Descripción
- Implante osteoconductor derivado de tejido óseo humano, Clase III, producto estéril, libre de pirógenos.
- Obtenido principalmente de la zona diafisaria del hueso tibial.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto liofilizado con una caducidad de 36 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para relleno de defectos y cavidades óseas en procedimientos quirúrgicos, en traumatología y ortopedia.
- Reconstrucción de fracturas por perdida de sustancia ósea
- Cirugía revisión de cadera
Código de Producto
- 16272210- Tira (barra) cortical 90-110L x 9-11W mm
- 16272215- Tira (barra) cortical ≥111-160L x 9-11W mm
- 16272220- Tira (barra) cortical ≥161-220L x 9-11W mm
- 16272410- Tira (barra) cortical 90-110L x 14-16W mm
- 16272415- Tira (barra) cortical ≥111-160L x 14-16W mm
- 16272420- Tira (barra) cortical ≥161-220L x 14-16W mm
- 16272610- Tira (barra) cortical 90-110L x 18-20W mm
- 16272615- Tira (barra) cortical ≥111-160L x 18-20W mm
- 16272620- Tira (barra) cortical ≥161-220L x 18-20W mm
Tendón Procesado Biograft
Registro Sanitario: 0746C2007 SSA
Descripción
- El tendón procesado Biograft® es un dispositivo médico, Clase III, derivados de tejido tendinoso humano, es estéril y libre de pirógenos.
- Compuesto por 90% de colágeno y 10% de Elastina.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto congelado con una caducidad de 48 meses almacenado a -40ºC.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de ligamento cruzado
Código de Producto
- 16002993- Tendón tibial anterior
- 16002994- Tendón tibial posterior
- 16560000- Tendón semitendinoso
- 16570000- Tendón gracilis
- 16580000- Tendón peroneal largo
- 16590000- Tendón peroneal corto
- 16600000- Tendón flexor común de los dedos
- 16610000- Tendón flexor de halux
Tendón de Aquiles
Registro Sanitario: 0746C2007 SSA
Descripción
- El tendón de Aquiles es un dispositivo médico, Clase III, derivado de tejido tendinoso humano, es estéril y libre de pirógenos.
- Compuesto por una pastilla ósea del hueso calcáneo y una sección tendinosa compuesta por 90%
- de colágeno y 10% de elastina.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto congelado con una caducidad de 48 meses almacenado a -40ºC.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de ligamento cruzado
- Reconstrucción de ligamento colateral
- Reconstrucción de Aquiles
Código de Producto
- 16450101- Tendón de Aquiles con calcáneo T=>180 mm
- 16450102- Hemitendón de Aquiles con calcáneo BO modelado
Tendón Hueso HTH
Registro Sanitario: 0746C2007 SSA
Descripción
- El tendón HTH es un dispositivo médico, Clase III, derivado de tejido tendinoso humano, es estéril y libre de pirógenos.
- Compuesto por dos pastillas óseas, una del hueso tibial y otra del hueso patelar unidas por una sección tendinosa del tendón patelar.
- La sección tendinosa está compuesta por 90% de colágeno y 10% de elastina.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto congelado con una caducidad de 48 meses almacenado a -40ºC.
- Contactar a Biograft® con el fin de obtener información sobre su conservación y logística de transporte.
Aplicaciones
- Reconstrucción de ligamento cruzado
Código de Producto
- 16500101- Tendón hemipatelar (HTH)
Fascia Lata
Registro Sanitario: 0746C2007 SSA
Descripción
- La fascia lata es un dispositivo médico, Clase III, derivado de tejido de fascia lata humano, es estéril y libre de pirógenos.
- Esterilizado mediante radiación gamma a una dosis mínima de 50 kg y mediante el Proceso Clearant®.
- Producto liofilizado con una caducidad de 48 meses y que puede ser almacenado a temperatura ambiente.
Aplicaciones
- Indicado para en procedimientos quirúrgicos en el área dental, maxilofacial, ortopedia y traumatología
- Como membrana biológica
Código de Producto
- 16480000- Fascia lata
- 16481520- Fascia lata ≥15 X ≥20 mm
- 16482130- Fascia lata ≥21 X ≥30 mm
- 16483140- Fascia lata ≥31 X ≥40 mm
Matriz dérmica acelular
Registro Sanitario: Nº 047C2016 SSA
Descripción
BioXiliumQ® Es un Aloinjertos de Matriz Dérmica Acelular resistente y flexible después de su reconstitución. BioXiliumQ® Esta envuelta en una membana de algodón y preservada en glicerol dentro de una bolsa perfecseal que esta dentro de una bolsa aluminzada.BioXiliumQ®No contiene componentes celulares ni sustancias potencialmente infecciosas ya que es esterilizada con bajas dosis de irradiación para garantizar su esterilidad y seguridad. A su vez se conservan sus cualidades biológicas y su estructura natural de colágeno Tipo I.
Después de su colocación BioXiliumQ® funciona como una apósito temporal que se revasculariza con rapidez. Se integrará sucesivamente en el tejido del organismo huésped y finalmente se reemplazará por tejido autólogo.
Aplicaciones
- Quemaduras térmicas de primer y segundo grado superficiales y/o profundas.
- Quemaduras químicas.
Código de Producto
| 17010010 | Matriz dérmica acelular sin mallar de 7A x 10L cm |
| 17010011 | Matriz dérmica acelular sin mallar de 7A x 15L cm |
| 17010012 | Matriz dérmica acelular sin mallar de 7A x 20L cm |
Matriz dérmica acelular

Registro Sanitario: Nº 047C2016SSA
Descripción
BioXiliumH® Es un Aloinjertos de Matriz Dérmica Acelular resistente y flexible después de su reconstitución. BioXiliumH® Esta envuelta en una membana de algodón y preservada en glicerol dentro de una bolsa perfecseal que esta dentro de una bolsa aluminzada.BioXiliumH®No contiene componentes celulares ni sustancias potencialmente infecciosas ya que es esterilizada con bajas dosis de irradiación para garantizar su esterilidad y seguridad. A su vez se conservan sus cualidades biológicas y su estructura natural de colágeno Tipo I.
Después de su colocación BioXiliumH® funciona como una apósito temporal que se revasculariza con rapidez. Se integrará sucesivamente en el tejido del organismo huésped y finalmente se reemplazará por tejido autólogo.
Aplicaciones
- Úlceras Cutáneas
- Úlceras por presión
- Úlceras venosas
Código de Producto
17010006 Matriz dérmica acelular sin mallar de 7A X6L cm
17010007 Matriz dérmica acelular sin mallar de 7A X7L cm
17010008 Matriz dérmica acelular sin mallar de 7A X8L cm
17010009 Matriz dérmica acelular sin mallar de 7A X9L cm
Cartílago Procesado
Registro Sanitario: Nº 0957C2013 SSA
Descripción
BioBrick® Aloinjerto de Matriz Hialiana derivada de cartílago costal procesado y estéril.
- Se integra con facilidad al organismo sin generar rechazo.
- Facilita el proceso de regeneración ósea debido a la presencia de colágeno y Factores de Crecimiento.
- Esta empacado en solución isotónica con glicerol.
- Almacenamineto a -40ºC
Aplicaciones
BioBrick ® se emplea en:
- Cirugía plástica Dorso Nasal.
- Rino Septum plastia.
- Auriculopastia.
- Implantología Oral.
- Reparación de defectos de mandíbula o maxilar.
- Plastia de pabellón auricular.
- Plastia de mentón.
- Reconstrucción de labio paladar hendido.
- Aumento de reborde óseo.
Código de Producto
| 16900001 | Membrana derivada de cartílago humano < 30 x > 4mm |
| 16900002 | Membrana derivada de cartílago humano > 30 x > 4 mm |
| 16902001 | Tira derivada de cartílago humano < 20 x > 7 mm |
| 16902002 | Tira derivada de cartílago humano 20 – 35 x > 7 mm |
| 16902003 | Tira derivada de cartílago humano > 35 x > 7 mm |
| 16900401 | Granulado derivado de cartílago humano 1.0 cc |
| 16900402 | Granulado derivado de cartílago humano 2.0 cc |
Teléfono
Ubicación
Priv. Sonterra #4015
Col. Sonterra, CP 76235 Queretaro, Queretaro
Horario
L-S: 8am - 5pm
URGENCIAS